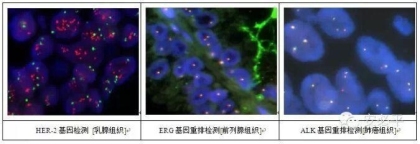
常规石蜡包埋组织切片(常规切片)是组织学常规制片技术中最为广泛应用的方法,在病理学中常用以研究、观察及判断细胞组织的形态变化,与免疫学技术结合可用于组织切片中细胞组织的多肽及蛋白质等大分子物质的定性和定位观察研究,与FISH方法结合可用于细胞中基因定位和状态分析,目前已广泛地用于多学科领域的研究中。
常规切片的FISH检测目前在临床逐渐开展,在分子病理中发挥的作用越来越大。例如,肺癌组织中ALK重排检测、乳腺癌样本中HER-2基因状态分析、淋巴瘤样本中各种原发和继发非随机克隆性细胞遗传学异常检测、软组织肉瘤诊断分型相关靶标检测等。FISH检测中,因为标本前期处理(固定、制片等)不当,或后续处理(煮片、消化等)失误造成的检测失败案例很多。因此,病理科在新开展FISH检测前往往要投入较多的时间、人力和物力进行培训,摸索适合本院样本的处理条件。
本篇总结了临床中常见的样本制备、处理过程中的关键点,提出适用于大多数常规切片的FISH样本处理标准方案,供大家实验中参考。
一、样本制备
常规切片的制备方法可以参考《临床技术操作规范•病理学分册》,新鲜样本取材后经过固定、水洗、脱水、透明、浸蜡、包埋、切片和烘烤制备成常规切片,过程中特别注意固定(固定液类型、固定时间)和切片(载玻片选择、预防脱片、切片厚度)。
1、固定
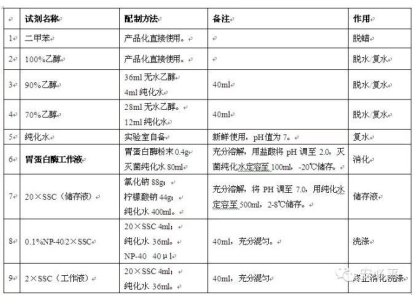
1) 固定液选择:常规固定液为4%中性甲醛(10%中性福尔马林),应预先多量配制贮存,以备随时使用,避免固定液PH值不准确、浓度不正确,影响固定效果。建议固定液配方:
|
福尔马林(40%甲醛) |
100ml |
|
磷酸二氢钠一水化合物 |
4.0g |
|
磷酸氢二钠(无水) |
6.5g |
|
蒸馏水 |
900ml |
2) 及时固定:凡需要进行病理组织学检查的标本(器官或组织),于离体(活体或尸体)后,应尽快置放(浸泡)于装有足够量固定液的容器中固定。固定液量应为被固定标本体积的5~10倍。固定不及时,细胞发生自溶,DNA降解,DAPI下观察,标本呈现核很浅,甚至有糜烂现象,信号无或缺失严重。
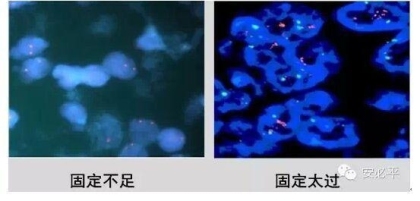
3) 充分固定:小标本的固定时间为4~6小时,大标本为18~24小时,不宜超过48小时。若固定不充分,信号可能很大比例的丢失;若固定时间太久,大分子交联情况严重,很难进行消化,背景高。如果把握不好固定的时间,对后续结果判读有很大的影响。
案例:
固定时间差异对FISH检测结果的影响非常明显,核形态差、信号亮度减弱,这部分样本往往需要进行强度更大的处理才能满足判读要求。
2、切片
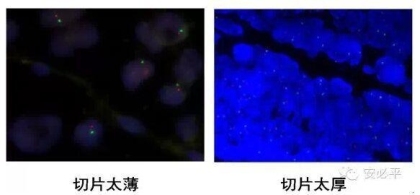
厚度:一般3 ~ 5μm之间,我们推荐第一次检测时分别制备3μm、4μm、5μm常规切片进行选择。若切片薄,消化时间相对短,若消化过度,信号会出现很大比例的丢失,影响结果判读;若切片厚,难于消化,需适度延长消化时间,且易出现细胞堆积层叠情况,细胞界限不清晰,不易单独计数,更易出现高背景,影响结果判读。
防脱片:选择防脱载玻片,且在捞片后,进行56℃过夜烤片(或者65℃烤片2小时)避免在后续样本处理过程中,出现脱片情况。载玻片的选择非常重要,建议预实验中进行对比测试,选择无自发荧光、背景干净、粘附效果好的载玻片进行FISH操作。
案例:
切片厚度比较容易确定,选择待检测样本,按梯度时间消化,杂交探针或直接进行DAPI复染判断消化状态。厚度理想,消化适中的样本应该核边界清晰,无层叠及成片现象,也不会出现似掉片的影状染色。
二、样本处理
常规切片样本制备完毕,接下来进行样本处理。
1、仪器/试剂/耗材
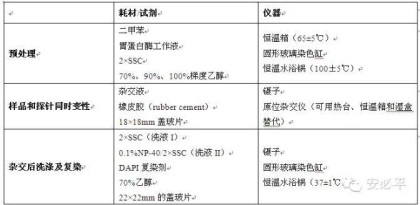
2、操作流程:
1) 预处理:

2) 杂交:

3) 洗涤:撕去封片胶,揭去盖玻片

4) 复染:滴加10μl DAPI复染剂至干燥的盖玻片上,反转样本片,使盖玻片分别与载玻片的目标区域接触,反转后轻压,避免产生气泡,在暗处存放,待观察。
注意事项:
1) 二甲苯对人体伤害很大,注意防护,可选用环保脱蜡剂替代二甲苯
2) 未特别注明温度,则为室温环境操作;非室温溶液,在操作开始前需提前预热反应试剂至指定温度。
3) 步骤2)-4)为避光操作
4) 初次操作,请参考相关说明书
5) 试剂配制应在通风柜内进行。
6) 配好试剂每周更换一次或用于20张玻片杂交后应更换,若试剂出现混浊或污染,请立即更换。
影响实验结果的关键因素
1) 脱蜡:要彻底,脱蜡不足,后续实验步骤都无法补救过来,导致背景高甚至探针杂交失败。重要但很容易办到(如利用午休时间脱蜡)。
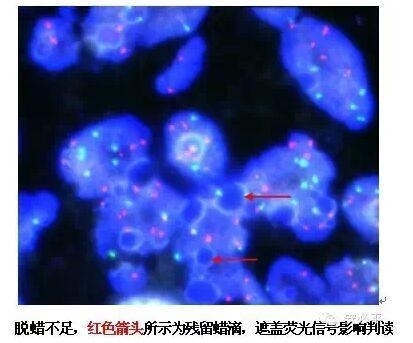
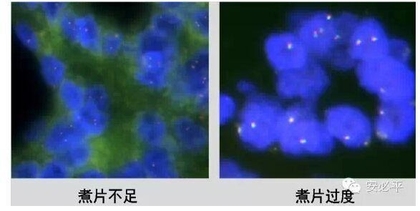
2) 煮片:保证时间25min钟左右,水温100±5℃。(水不宜爆沸,有造成脱片的可能。如电磁炉煮片,可煮开后降低功率加入标本煮片,开始计时)。煮片时间不足,蛋白交联没有充分去除;煮片时间过长,细胞核粘连严重,影响计数判读。
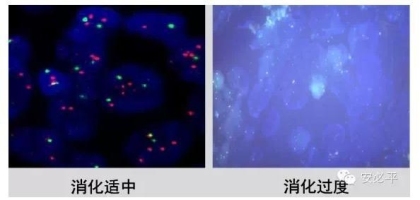
3) 酶消化:消化时间的确定需要通过预实验摸索。如果消化不足(酶浓度低、温度不适合、时间太短),镜下会出现云雾状组织覆盖在细胞上,无法观测到暴露独立的细胞核,从而降低杂交效率并很难选择细胞进行计数;如果消化过度,则细胞核被损伤,失去正常的圆形完整形状,核物质丢失,影响结果判读。
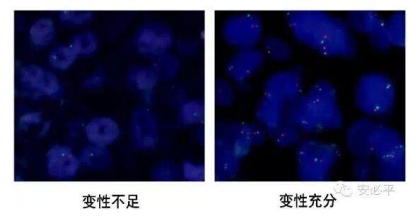
4) 变性:变性是利用高温打开探针和标本DNA双链,然后降温后彼此才能互相配对杂交。变性温度要准确,恒定。变性温度、时间不够,探针DNA和靶DNA未充分打开,杂交效率自然很低,会出现信号弱,或无信号的情况。因此需要确保变性温度及时间充足。
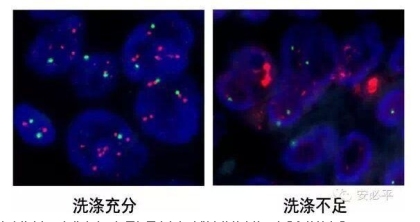
5) 杂交后洗涤:确保温度、SSC浓度、去垢剂、pH值等条件的准确性。杂交后洗涤可以去除未杂交探针和非特异杂交信号。尤其是着丝粒探针,通常会产生很强的荧光信号,若洗涤不够会出现高背景的情况。所以要确保洗涤温度和洗涤时间。
通过上述的介绍,相信大家已经了解了常规切片样本的基本处理步骤和关键步骤。
日常实验操作中,只要注意上述提到的关键点,相信大家也一定可以做出漂亮的样本片!
附录:主要试剂配制表: