就看着大家一直在问WB的内参咋调啊,上样量总是不齐啊咋办。我想说,你们还是太保守了……WB就光是调内参的事么?于是夏老师就随便找了篇9.517分的Sci Signal,给你们上一课:

首先,第一点,WB样本的准备。是不是都觉得不算啥问题?就裂解液一裂解就行了?

最常用的裂解液事RIPA缓冲液,一般会含有SDS和脱氧胆酸钠,这都是蛋白去污剂。但是即使是这样,缓冲液都会产生不溶性部分。他们分析了RIPA裂解后的上清(Sup)以及不溶性颗粒(Pel)中的WB,结果发现:
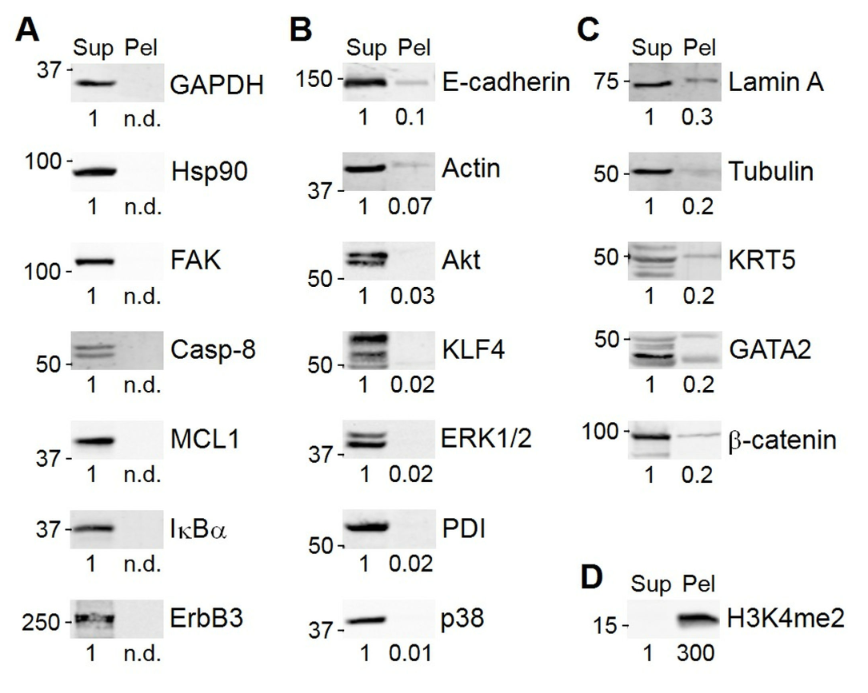
看到了?H3K4二甲基化的蛋白,几乎不能溶解……其他也有一些蛋白,是部分溶解在上清中的。
而不同的裂解液,可能也对最终的结果产生影响。这里他们用RIPA裂解缓冲液、NP40裂解缓冲液(缺乏 SDS 和脱氧胆酸盐)和 Laemmli 样品裂解缓冲液(含有二硫苏糖醇)分析。他们首先激活了FAS,促进凋亡激活。这个还记得么?给你们讲过的喔……
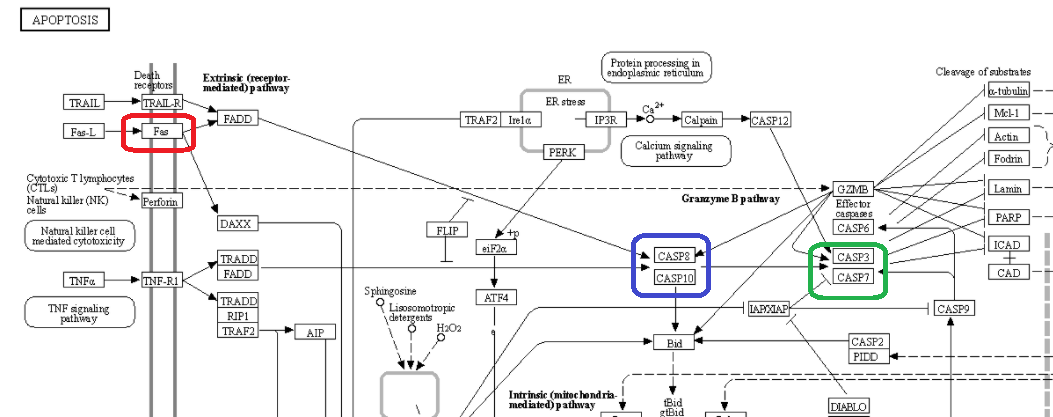
凋亡激活后,下游的Caspase3和Caspase8会被剪切成成熟体。但是不同的裂解液,最终会导致剪切后的成熟体检测结果不同:
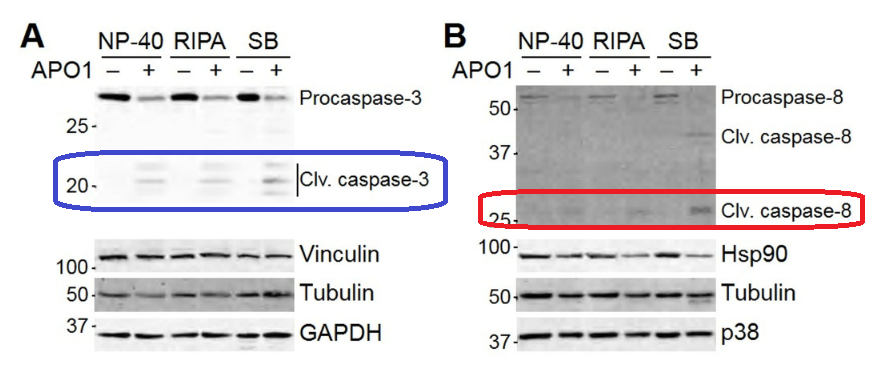
只有 Laemmli 样品裂解缓冲液处理,才能检测到有成熟体的Caspase8。所以,裂解缓冲液有多重要,直接能影响你的检测结果。
有时大家会认为 RIPA 中的 SDS 和脱氧胆酸盐会使大多数细胞酶失活。所以在做磷酸化WB的时候,不再加磷酸酶抑制剂……但实际上结果是:
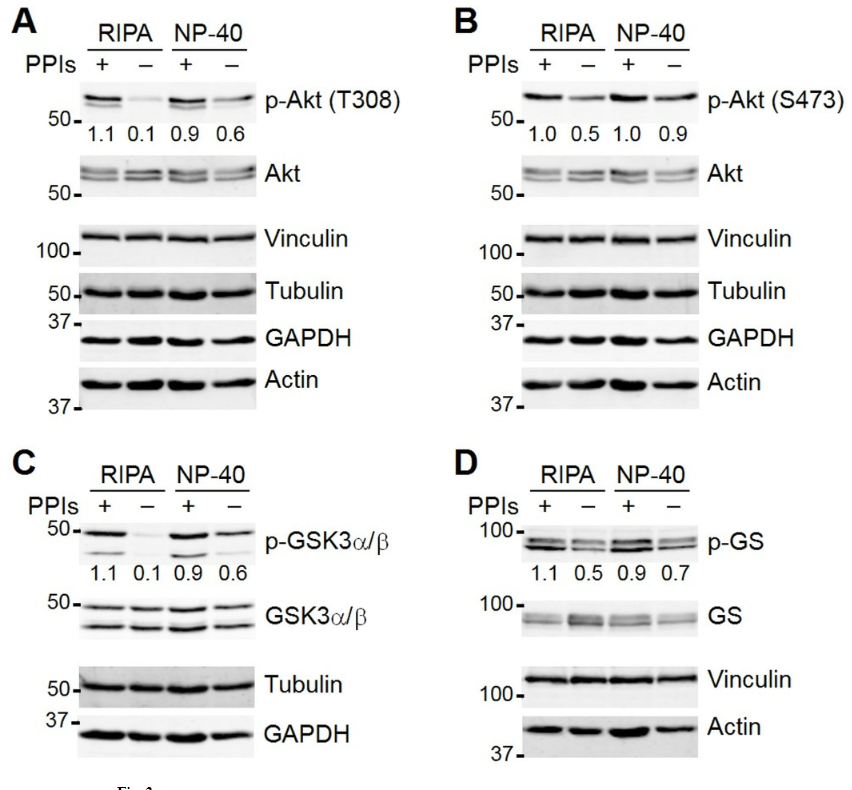
很明显,只有加入了磷酸酶抑制剂,才能获得更好的磷酸化WB的结果。
对于WB,是不存在适用于所有电泳转移设置和检测方法的单一方案的。所以刚开始预实验,就先要通过样本的连续稀释,找到最佳的上样量:
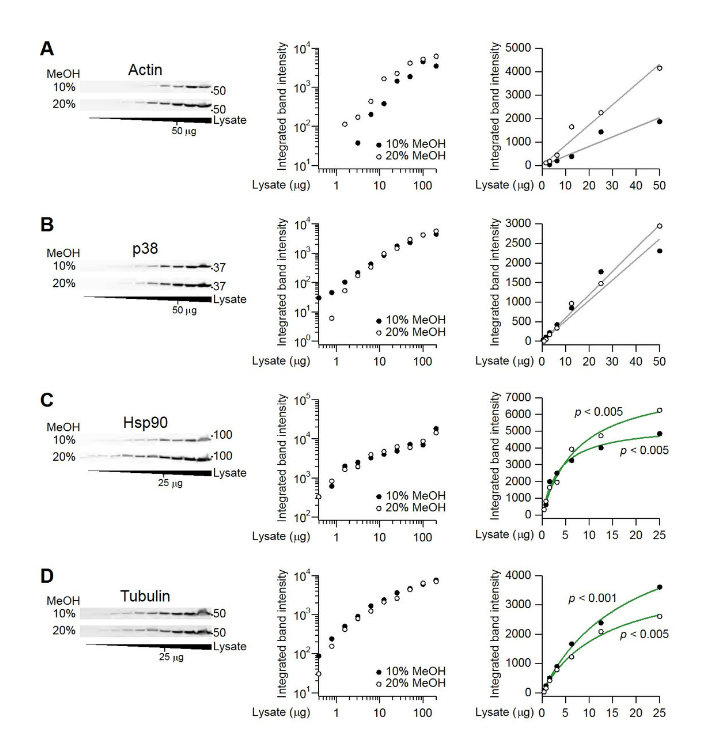
如果是线性的,就还好,但如果是指数型或者幂函数曲线,就需要取较为线性的区段中的上样量了:
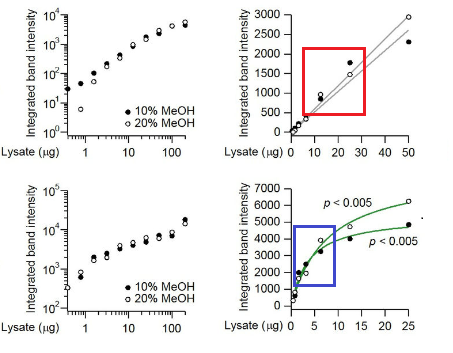
除了这些,甚至不同的WB发光成像试剂,对于不同的蛋白,都会有不同的线性结果:
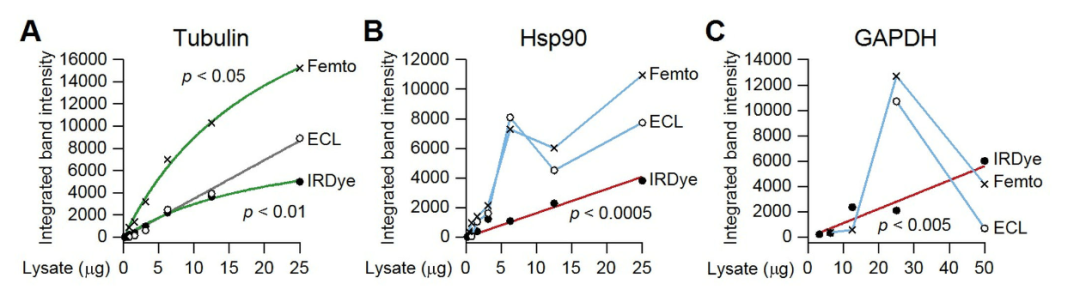
最后样本结果需要稳定,合适的内参选择也很重要,这个之前也给你们介绍过,如何选择WB的内参了。好的内参,在样本间的CV值较低。
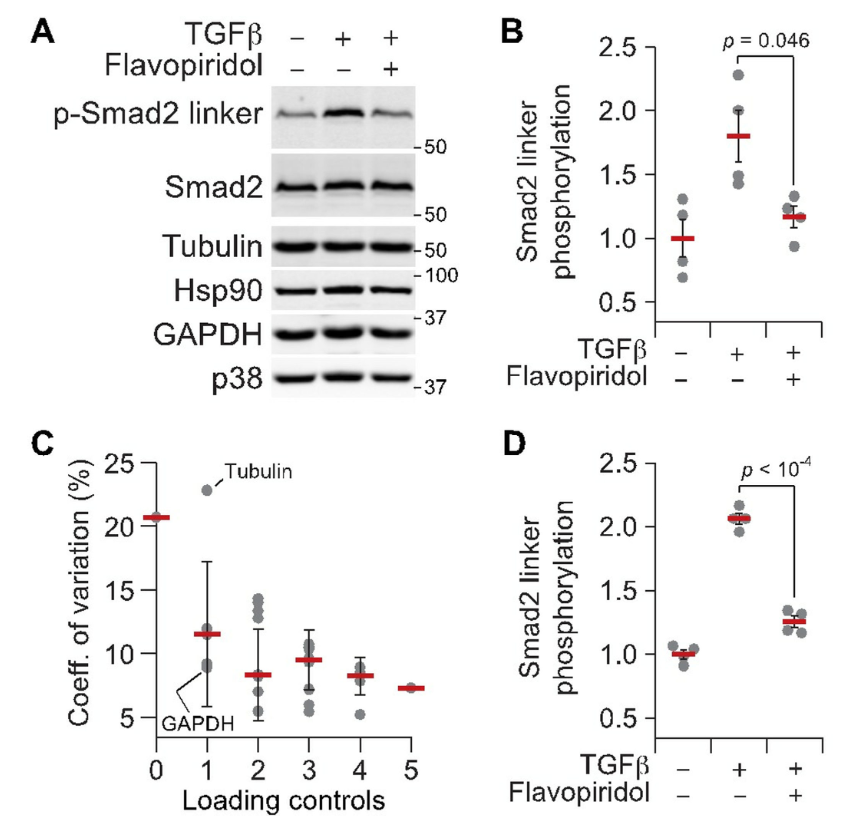
其实很多文献都建议用总蛋白含量来代替内参,可以获得更稳定的结果。