在细胞死亡领域,各种细胞死亡方式的研究在近两年的火热程度可谓有目共睹,尤其是最新出现的铜死亡,出现之初几乎是蜂拥而上,各种文章层出不穷。
失巢凋亡?是什么东西?你看看,问题这就来了
细胞与细胞外基质(ECM)粘附丧失或粘附不当定义为“失巢”,正常上皮细胞一旦失去与ECM的接触就会迅速发生凋亡,这就是失巢凋亡。失巢凋亡是由于细胞脱离细胞外基质而启动的特殊的程序性细胞凋亡,在机体发育、组织自身平衡、疾病发生和肿瘤转移等方面起重要作用。当细胞失去与ECM的附着时,系留在细胞骨架上的促凋亡蛋白Bmf与动力蛋白轻链2发生解离,易位到线粒体,从而促进失巢凋亡的发生。
然而,肿瘤发展和生长的一个共同特征是在“独立”的生长条件下转化细胞的生存能力。这种对失巢凋亡的抵抗已经被证实与细胞内环境稳态丧失、癌症生长和转移有关,这种获得的能力被称为失巢凋亡抗性。具有抗失巢凋亡的癌细胞可以通过外周循环系统扩散到远处的组织或器官并导致癌症转移。研究控制抗失巢凋亡的分子机制将有助于探寻人类恶性肿瘤的有效疗法。
失巢凋亡激活机制
正常情况下,缺乏ECM接触或与不适当的ECM接触不能激活促生存信号,导致抗凋亡通路的减少,从而通过死亡受体和线粒体激活失巢凋亡。外部途径通过增加Fas死亡因子受体的表达而被激活,Fas受体的激活触发两种不同的外部途径:1型,导致依赖于caspase 7激活的靶点的直接蛋白水解;2型,通过t-Bid(Bid的截断形式)在内在途径上汇聚,促进线粒体细胞色素c的释放和凋亡小体的组装。内在途径是通过上调促凋亡分子(如Bad、Bik、Puma、Hrk、Bmf和Noxa)来诱导的,这些分子可以抑制Bcl-2家族的抗凋亡蛋白。这些过程诱导半胱天冬酶特异性靶蛋白,从而促进蛋白水解,从而促进失巢凋亡(图1)。
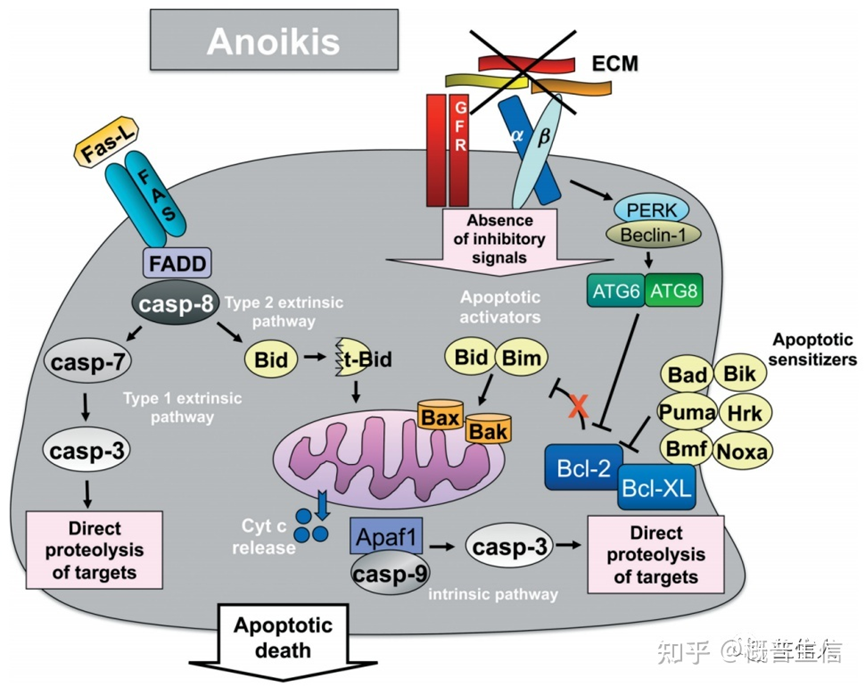
癌症中的抗失巢凋亡
与正常上皮细胞形成鲜明对比的是,癌细胞对失巢凋亡不敏感,不需要粘附ECM就能存活和增殖。这种能力在转移过程中有重要的意义,癌细胞必须在没有适当ECM接触的情况下存活和迁移。在这种情况下,失巢凋亡抗性是癌症侵袭性转移扩散的自然分子先决条件(图2)。
ECM的整合素参与通过激活关键参与者触发了多个促生存途径,最终导致Jun、Fos和NF-κB的转录;促凋亡蛋白被抑制,阻止细胞死亡的外在途径和内在途径;生长因子受体与整合素协同促进细胞存活,大部分集中在相同的途径(图3)。
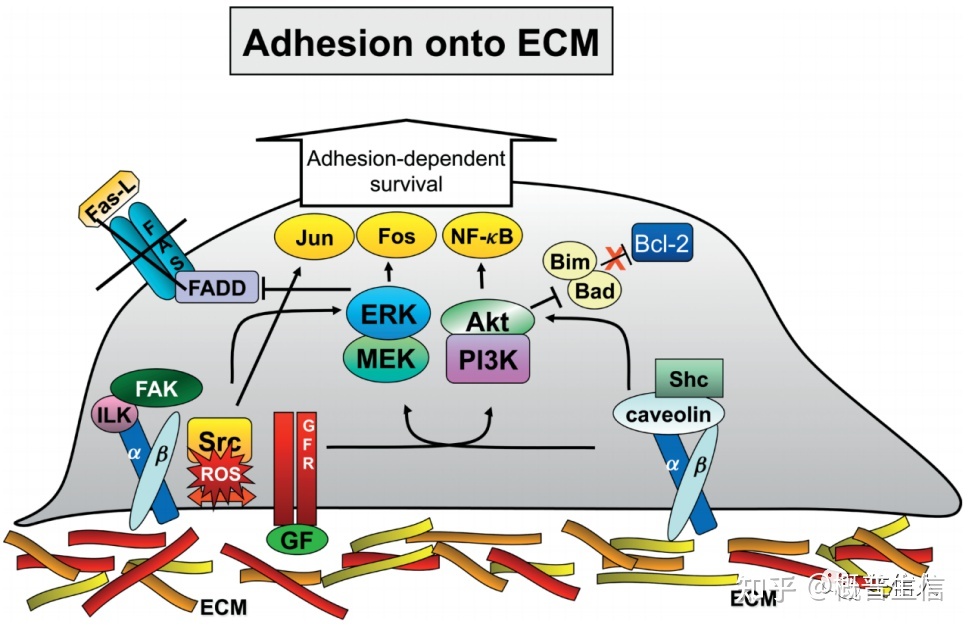
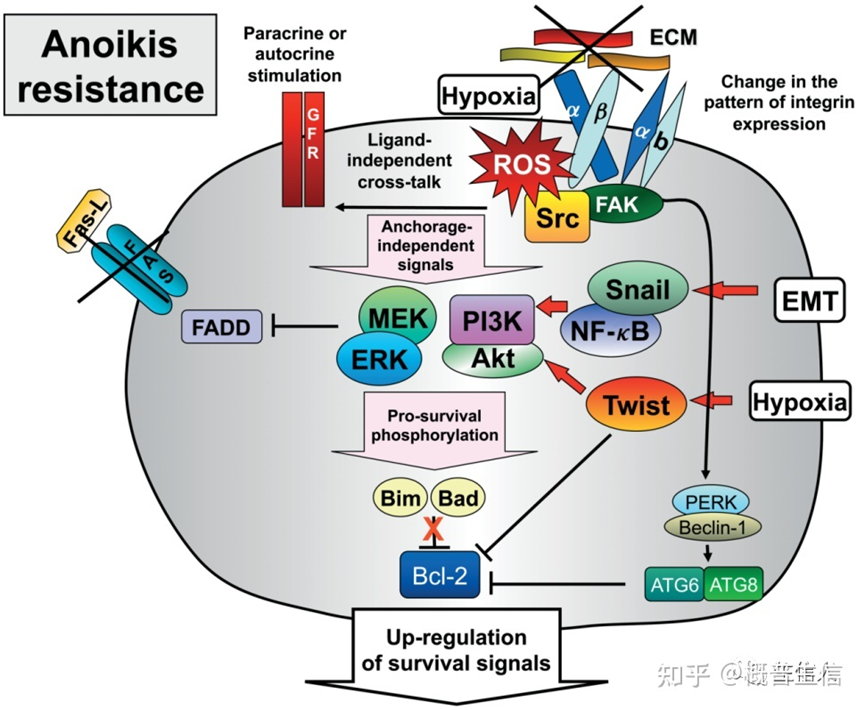
获得失巢凋亡抗性的途径
在病理情况下(如癌症),细胞可以避免失巢凋亡。由于有几种策略,癌细胞获得了失巢凋亡抗性,允许它们存活,并在远处的组织中定植。细胞防止失巢凋亡的几种策略,集中在生存信号的激活和抑制死亡途径上:
- 由于自分泌生长因子环或邻近细胞的旁分泌刺激,细胞可以通过激活促生存途径来避免失巢凋亡;
- 细胞会改变整合素的表达模式,以便它们能够接收到正确的环境生存信号;
- 在高水平的ROS下生长因子受体的非配体激活,缺氧通过氧化还原介导的促凋亡因子的下调,进一步增加了ROS的产生和对失巢凋亡的保护;
- EMT的激活,导致生存级联激活的几种转录因子(Snail,Twist,NF-κB)的上调对于EMT的成功和抗失巢凋亡至关重要;
- 缺氧也可以通过激活Twist转录因子来发挥作用,进而激活EMT程序。
至此,癌细胞无视失巢凋亡脱离ECM“远走高飞”(图4)。
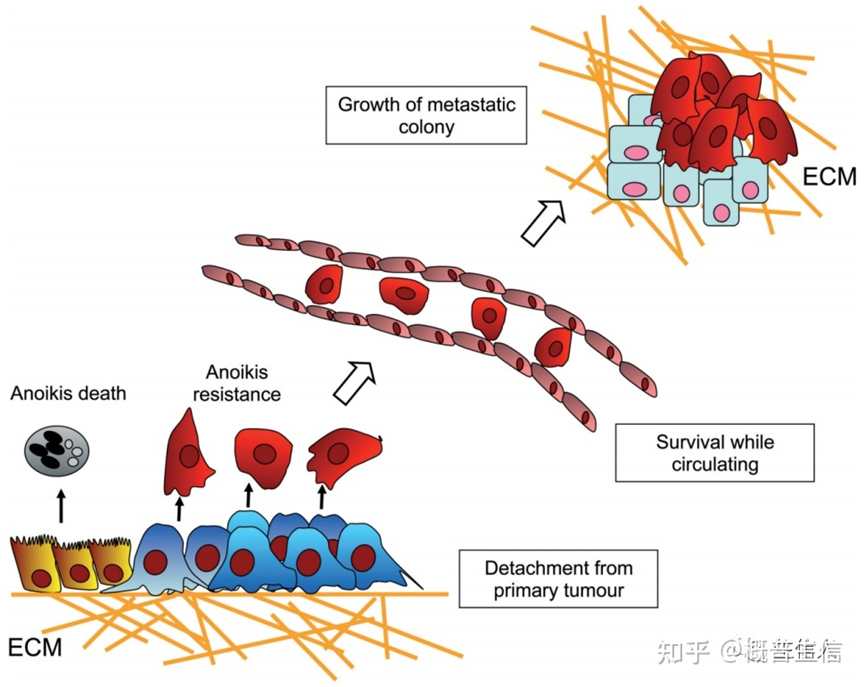
近十年有关于失巢凋亡的文章稳定在每年150篇左右,一直被默默地持续关注着,就像金子一直在某一处发着光直到有一天被挖掘被知晓,但是这不妨碍它是块“金子”。按照惯例,一个被关注新的热点出现的时候(比如铜死亡),发文量最先被生信文章占领,因为它快,而后才是实验为主的文章,然后可能就是综述类;而当一些一直未被众人知晓的点被实验性文章所囊括,这就说明它真的是值得深究的问题,而在达到一定程度之后生信文章也会慢慢出来,然后层出不穷。失巢凋亡恰恰是后者。